

 0
Сравнивать
0
Сравнивать
 Пользователь
Пользователь
 0
Корзина
0
Корзина

pH measurement
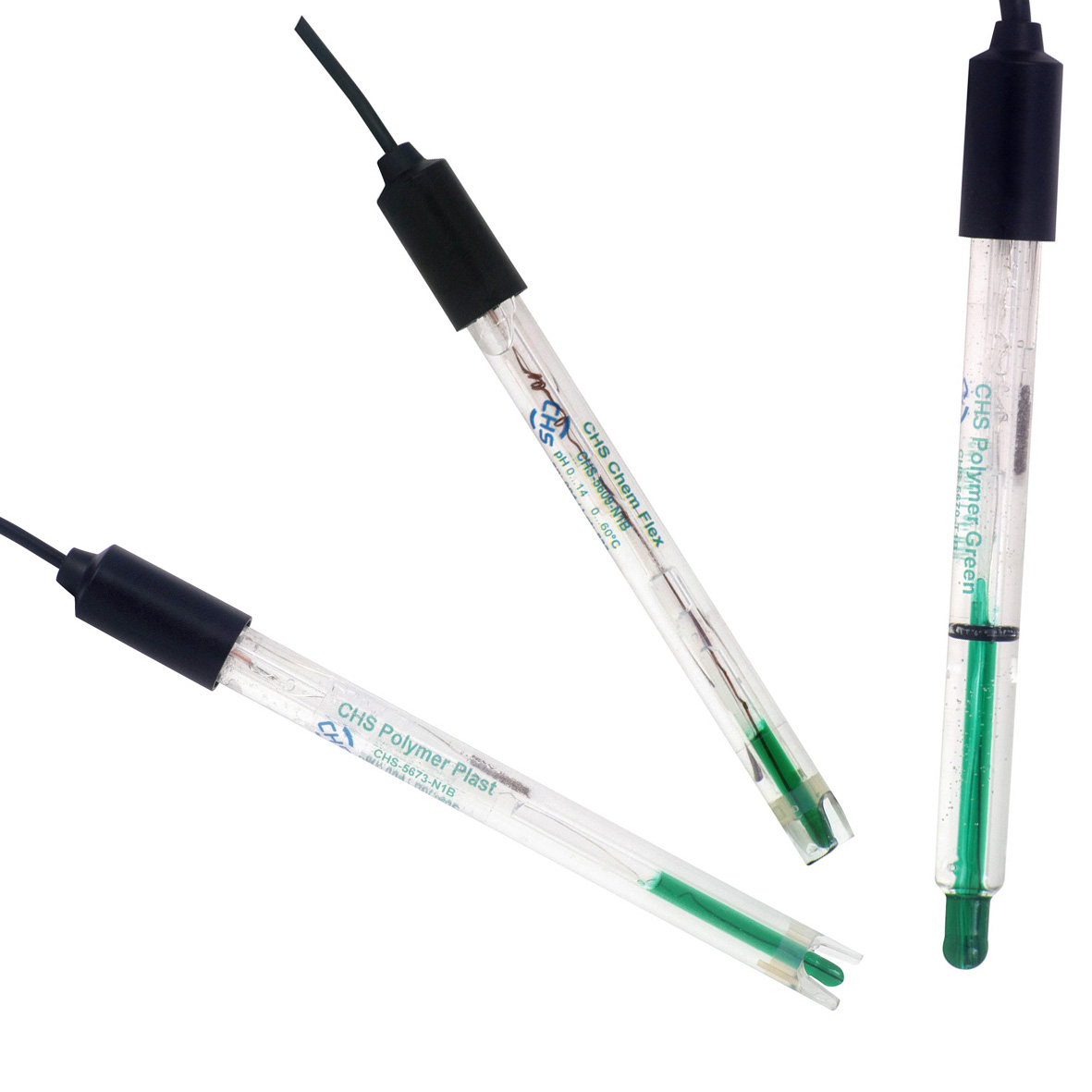 Измерение pH
Измерение pH
Определение значений pH основано на принципе потенциометрического измерения – измерения электрического напряжения. рН-электрод состоит из двух электродов (рН-стеклянная мембрана и эталонный), которые объединены в одно устройство в составе комбинированного рН-электрода. Между этими двумя электродами измеряется напряжение. pH-мембрана электрода изготовлена из специального непроницаемого и электрически изолированного стекла. Это стекло (pH-стекло) образует гидратированный слой в воде и избирательно реагирует на ионы водорода (H+). Ионы натрия (Na+) в стекле замещаются ионами водорода (H+), что вызывает изменение свободной энергии и электрического потенциала, измеряемого рН-метром. Количество обмена Na+ и H+ через стекло pH сильно зависит от pH раствора. Чем выше pH, тем меньше ионов водорода в растворе, поэтому меньше ионов натрия замещается через pH-стекло. Жидкость внутри рН-стекла представляет собой буферный раствор с известной и постоянной концентрацией ионов водорода. В зависимости от разницы рН между внутренним буфером и измеряемым раствором между внутренним и внешним слоями рН-стекла возникает гальваническое напряжение. Это напряжение измеряется двумя электродами Ag/AgCl. один электрод расположен во внутреннем буфере, другой — в электролите сравнения. Большинство pH-электродов имеют почти линейную характеристику в диапазоне измерения pH от 0 до 14. Используя преимущества этого поведения, pH-электрод калибруется между двумя хорошо известными значениями pH, например, pH 4,01 и 7,00. Между этими двумя значениями проводится линейная экстраполяция, а также линейная интерполяция.



